L'enllaç Iònic
Perquè tingui lloc l'enllaç iònic hi ha d'haver una transferència d'electrons d'un àtom cap a un altre.
Ho veurem amb un exemple:
En el cas del NaCl, com que per separat el Cl és molt electronegatiu (X=3.0) i el Na és molt electropositiu (X=1.0), el Clor tindrà tendència a captar l'electró de valència del Sodi per tal d'omplir la seva última capa amb 8 electrons, transformant-se en l'anió Clorur, Cl-, i de la mateixa manera, el Sodi, quan hagi cedit el seu electró també tindrà 8 electrons a la seva última capa, passant a ser un catió de sodi, Na+. La interacció electrostàtica (atracció entre càrregues oposades) que es donarà entre catió i anió donarà lloc a un enllaç iònic molt estable entre els dos àtoms:
Cl (Z=17): 1s2, 2s2, 2p6, 3s2, 3p5 Cl-: 1s2, 2s2, 2p6, 3s2, 3p6
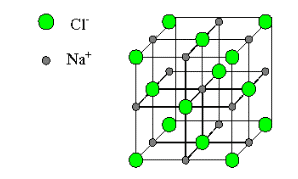
Na (Z=11): 1s2, 2s2, 2p6, 3s1 Na+: 1s2, 2s2, 2p6Ara bé, en realitat els compostos iònics no s'enllacen a un sol àtom, sino que formen xarxes cristal·lines iòniques i atrauen o cedeixen electrons en funció del nombre d'àtoms de l'element diferent que tinguin a la vora (això s'anomena número de coordinació). El NaCl, per exemple, té un número de coordinació 6:6, i això vol dir que cada àtom de Clor estarà envoltat de sis àtoms de Sodi a la xarxa cristal·lina, i viceversa, i que, per tant, el sodi no cedirà un electró a un clor, sinó 1/6 part de l'electró a cada àtom de clor que l'envolta, i de la mateixa manera, el clor, que tindrà 6 àtoms de sodi al voltant, omplirà la seva última capa amb un electró prenent 1/6 part de l'electró de cada un dels 6 àtoms que l'envolten (6 x 1/6 = 1).